Wizualnie czysto: wprowadzenie przejrzystości do przepisów
Autor: Thomas Altmann, Kierownik techniczny ds. globalnej walidacji mycia CIP/COP

Czystość wizualna jest terminem używanym w niemalże wszystkich regulacjach prawnych dotyczących branży farmaceutycznej (FDA, PIC/S, GMP). Mówiąc wprost, sprzęt używany w farmaceutycznych procesach produkcyjnych musi być sprawdzony wizualnie pod względem czystości przed użyciem1.
To logiczne, ale niewiele osób jest w 100% świadomych, co oznacza wizualna czystość w standardowych procedurach operacyjnych i jak należy je udokumentować w celu walidacji mycia. Do najczęściej zadawanych pytań należą:
- Jak wyglądają pozostałości?
- Co to jest próg wizualny?
- W jaki sposób materiał konstrukcyjny wpływa na widoczność?
- Jak często insepktorzy powinni badać wzrok?
Poniżej przedstawiam krótkie omówienie każdego z tych zagadnień.
Jak wyglądają pozostałości?
Podczas inspekcji sprzętu inspektorzy muszą wiedzieć, czego właściwie szukają. Powinni oni przynajmniej być w stanie rozróżnić pozostałości z procesów technologicznych od pozostałości po detergentach i środkach dezynfekcyjnych oraz określić, jak niskich poziomów każdego z tych rodzaju pozostałości można oczekiwać. Co więcej, inspektorzy muszą posiadać wiedzę na temat aspektów wizualnych czystej powierzchni, w tym zabarwienia stali, zarysowań lub innych uszkodzeń, które nie wpływają na kolejny etap produkcji.
Przykładowo, aktywne składniki farmaceutyczne (Active Pharmaceutical Ingredients, API) często występują w postaci proszków, a pozostałości detergentów mogą być widoczne jako plamy na powierzchni.

Pozostałości aktywnych składników farmaceutycznych często występują w postaci proszków.

Pozostałości detergentów często występują w postaci plam.
Pozostałości detergentów są często niezauważane przez inspektorów, którzy dokonują sprawdzenia, czy powierzchnia jest wizualnie czysta. Producenci farmaceutyczni stosujący środki przeznaczone do użytku w przemyśle spożywczym powinni być świadomi, że pozostałości składników nierozpuszczalnych w wodzie, takich jak inhibitory korozji lub specyficzne środki powierzchniowo czynne, mogą pozostawać na powierzchniach i powodować nieoczekiwane interakcje z pozostałościami substancji czynnych z procesów farmaceutycznych i mogą być przenoszone do kolejnych wytwarzanych produktów.
W jaki sposób materiał konstrukcyjny wpływa na widoczność?
Pozostałości mogą wyglądać inaczej w zależności od materiału użytego w procesie produkcyjnym sprzętu, który podlega inspekcji. Około 90% sprzętu używanego w procesach produkcyjnych w branży farmaceutycznej jest wykonane ze stali nierdzewnej, przy czym szkło, guma i polimery, takie jak Teflon i EPDM, stanowią większość pozostałej części.
Przy wyborze sprzętu i szkoleniu inspektorów należy mieć świadomość, że wykrycie pozostałości na powierzchniach polimerowych jest trudniejsze niż wykrycie pozostałości na sprzęcie wykonanym ze stali nierdzewnej.
Niemniej jednak sprzęt ze stali nierdzewnej wystawiony na działanie wysokiej temperatury może z czasem ulec odbarwieniom, co sprawia, że identyfikacja pozostałości jest trudniejsza w porównaniu z nowym sprzętem. Wszelkie powierzchnie sprzętu, które ulegną zarysowaniu, będą musiały zostać ponownie wypolerowane (jeśli jest to możliwe) lub wymienione na nowe, jeżeli pewna weryfikacja wizualnej czystości nie jest już możliwa.

Inspektorzy muszą zostać przeszkoleni, aby móc zidentyfikować każdy rodzaj pozostałości na wszystkich powierzchniach.

Na wygląd pozostałości mogą mieć wpływ różne wykończenia materiału (stal nierdzewna w porównaniu z teflonem lub nowa/wypolerowana stal w porównaniu z przebarwioną).
Co to jest próg wizualny?
Próg wizualny to poziom nagromadzenia pozostałości, przy którym aktywne składniki farmaceutyczne lub osady stają się widoczne. Producenci muszą określić próg wizualny dla każdego aktywnego składnika farmaceutycznego, a następnie porównać go z poziomem, przy którym dany składnik lub jego pozostałość staje się toksykologicznie znacząca. Jeśli próg wizualny jest niższy niż ustalony wcześniej poziom toksykologiczny dla danego aktywnego składnika farmaceutycznego lub pozostałości po myciu, wówczas potweirdzenie czystości wizualnej jest ważnym krokiem.
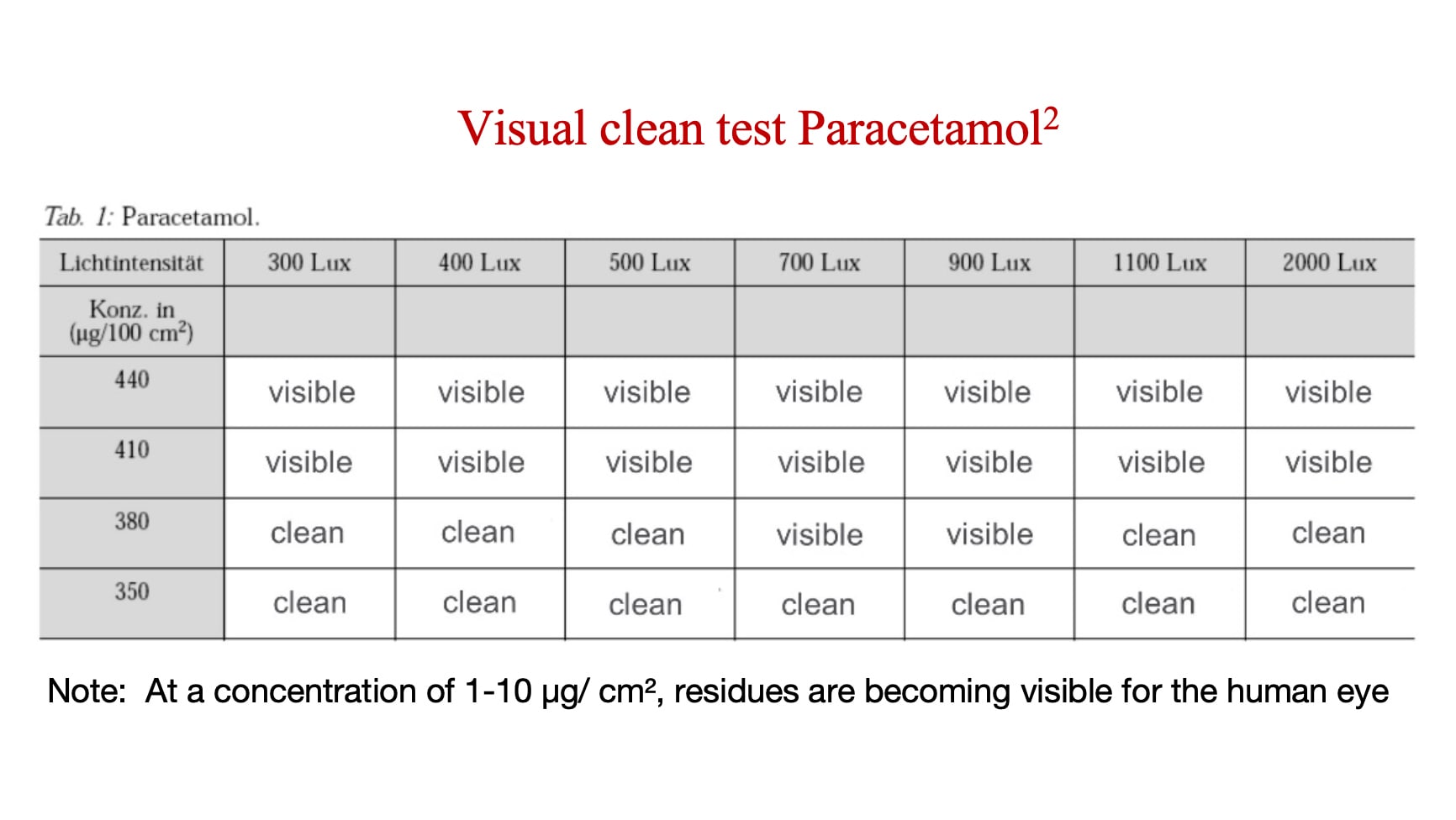
Poniższa analiza pokazuje stężenie, przy którym paracetamol (aktywny składnik farmaceutyczny o stosunkowo niskim ryzyku) staje się widoczny.
Jak często insepktorzy powinni badać wzrok?
Tutaj także brak jest szczegółowych wytycznych. Wiele firm wymaga obecnie, aby wszyscy inspektorzy przeprowadzający kontrole wizualne poddawali się badaniu wzroku corocznie.
Niemniej jednak nie jest to wymagane przez prawo. Z drugiej strony, jeśli procedury mycia zostaną zakwestionowane, udokumentowanie przeprowadzenia gruntownego szkolenia inspektorów oraz regularnych testów ich wzroku, aby przekonać agencje regulacyjne, że zrobiono wszystko, czego można racjonalnie oczekiwać, będzie trudne.
Pytania?
Aby uzyskać więcej informacji na temat najlepszych praktyk i wytycznych dotyczących czystości wizualnej, prosimy o kontakt z Ecolab Life Sciences. Jesteśmy obecni w zakładach farmaceutycznych na całym świecie i chętnie dostarczymy informacji o tym, jak inni producenci wdrożyli inspekcje czystości wizualnej do swoich programów walidacji mycia.
1FDA - CFR 21, Część 211,67 wymagana w punkcie (6) Kontrola czystości sprzętu bezpośrednio przed użyciem.
2Pharm. Ind. 62, Nr. 6 (2000) Buscalferri et al. − Reinigungsvalidierung


